За последние десятилетия своей карьеры я провел бесчисленное количество часов, защищая американцев, исследуя безопасность наркотиков. Мое образование и карьера позволили мне пройти через полдюжины университетов, Большую Фарму и FDA при трех президентских администрациях. Безопасность лекарств учитывает, почему один человек может принимать фармацевтический продукт и не иметь побочных эффектов, в то время как другой человек может принимать тот же продукт, но иметь побочные реакции вплоть до постоянной инвалидности или смерти. По умолчанию при изучении безопасности лекарств также учитываются доклинические аспекты производства и качества лекарств.
Поскольку качество лекарств является важным фактором при оценке безопасности лекарств, мой путь по защите американцев привел к разработке концепции и созданию первой в миреаналитическая аптекаМиссия компании заключалась в научной проверке фармацевтической продукции из таких стран, как Индия и Китай, прежде чем раздавать ее пациентам. К сожалению, стремление к щедрости в ущерб этике и защите пациентов привело к тому, что финансовое руководство этой компании взяло на себя обязательство обширный Нарушения FDA и быть обвиненным судьями в совершении ложные научные утверждения (все это случайно произошло после моего ухода).
Без внешнего подтверждения качества лекарств американцы полностью зависят от FDA и производителей в оценке и подтверждении чистоты продукта. Было доказано, что безопасность лекарств является заслуживающей внимания проблемой, когда речь идет об инъекциях мРНК Covid. К сожалению, если кто-то захочет провести собственный анализ инъекций мРНК, он у вас нет достаточно подробного списка ингредиентов для его сравнения или даже доступа к установленной нормативной методологии о том, как правильно проверить его на чистоту..
Это потому, что производители и FDA рассматривает все ингредиенты этих инъекций мРНК, включая последовательность мРНК и свойства липидных наночастиц (ЛНЧ), включая период полураспада, структуры ЛНП, поверхностные модификации, количество/типы ЛНП на дозу и точки прикрепления на цепь мРНК не указана или является «коммерческой тайной».
Кроме того, FDA дополнительно рассматривает методологии о том, как проверять инъекции мРНК на чистоту, также является коммерческой тайной.
Двухпартийная поддержка и сотни миллиардов долларов налогоплательщиков, но НЕТ прозрачности?
Секретность мРНК Covid существует даже несмотря на то, что администрации Трампа и Байдена предлагали полную прозрачность при инъекциях мРНК вплоть до отмены прав интеллектуальной собственности на мРНК Covid. Несмотря на это, и FDA, и производители строго контролируют патенты, включая основные данные об этих уколах, как коммерческую тайну. Они делают это, несмотря на то, что все производители вакцин против Covid получили сотни миллионов долларов налогоплательщиков по данным Форбс/Статиста публикации.
Изучать эпидемиологию безопасности лекарств достаточно сложно. Без поддающейся проверке чистоты/согласованности продукта полная оценка безопасности невозможна.
Полная прозрачность всех ингредиентов и меры контроля качества важны не только потому, что они в значительной степени финансировались налогоплательщиками в виде сотен миллионов долларов, но и потому, что возникло множество вопросов о безопасности и эффективности инъекций мРНК Covid.
Помимо того, что они были исключительно сложными, их одобрение было ускорено регулирующими органами после менее одного года. Большинство лекарств и вакцин обычно занимают около десять лет для полной проверки безопасности/эффективности, рассмотрения и утверждения. Помимо того, что ингредиенты являются совершенно новыми, очень сложными и первыми в своем роде, которые применяются в массовом масштабе, разработка включает в себя долгосрочные оценки клинической безопасности/токсичности и эпидемиологические обзоры были ускорены и, вероятно, не были полностью выяснены до выпуска.
Проверка ингредиентов, прозрачность и «правдивость» FDA имеют прецеденты, относящиеся к 1800-м годам:
Аналитическая проверка и прозрачность ингредиентов или «правдивость маркировки», когда указано содержимое бутылки. обязательный соответствовать перечисленным ингредиентам до создания FDA, в 1862 году.. Сегодняшнее FDA фактически родилось из того, что начиналось с одного сотрудника «Департамента химии», работавшего в Министерстве сельского хозяйства США.
фальсификация, (измененные или токсичные ингредиенты) неправильный брендинг (содержит ложную этикетку или иным образом вводит в заблуждение или содержит неверные медицинские утверждения), или неправильная маркировка (содержит ингредиенты, не указанные на этикетке продукта) имеют долгую и ужасную историю в Америке. Считалось, что пик этой вопиющей вопиющей ситуации пришелся на начало-середину 19-го века – или, по крайней мере, именно тогда она стала заметной – поскольку только к 1862 году были разработаны технические процессы для анализа и обнаружения подделки ингредиентов. До этого так называемые «странствующие знахари», называющие себя «докторами» (неизменно с сомнительными или несуществующими полномочиями), торговали бутылками с «панацеей от всех болезней», на этикетках ингредиентов которых было указано лишь туманное или безобидное содержимое, например: «витамины"экстракты трав,, либозмеиное масло»- или часто вообще не имеют списка ингредиентов.
В то время многие набожные пуритане Новой Англии, которые по религиозным причинам никогда прикоснувшись к алкоголю, купил бы эти растворы у этих торговцев-торговцев и неосознанно был бы обманут, заставив их употреблять растворы, которые содержали не только алкоголь, но и наркотики, такие как опиум и / или кокаин. Под предлогом облегчения нелепо широкого спектра недугов у пациентов вместо этого развивалась карательная зависимость и/или иным образом на их здоровье негативно влияли эти первые «торговцы наркотиками».
По мере того, как проблема росла, федеральное правительство начало обращать на нее внимание. В конце концов, Закон о чистой пище и наркотиках был принят в 1906 году и привел к созданию Управления по контролю за продуктами и лекарствами (FDA).
[У FDA было обучение обязанность гарантировать, что лекарства имеют правдивую информацию на этикетке и соответствуют определенным стандартам чистоты и силы.
Помните, что почти 120-летний требование правдивой маркировки и часть «чистоты» Закона о чистых продуктах питания и лекарствах 1906 года, когда вы читаете о проверочном тестировании мРНК и прозрачности ингредиентов.]
Какие «правдивые» и «чистые» проверочные испытания ингредиентов проводятся для продуктов, регулируемых FDA?
Еще в 2021 году FDA решило начать мониторинг качества фармацевтических препаратов в Америке с помощью удаленная коллекция of отправка образцов по почте на лекарства вместо проверок объектов в реальном времени из-за пандемии Covid. Это было законно? Можно ли когда-нибудь считать это научно обоснованным? Сегодня, несмотря на то, что пандемия закончилась, единственное официальное тестирование выпуска фармацевтической продукции, которое в настоящее время проводится на любой Фармацевтическая мРНК Covid появляется в все еще быть выполнено FDA через поставляемый производителем продукт»,отправлено по почте» образец в соответствии с снимок экрана текущего веб-сайта FDA. Очевидно, что метод отбора проб «по почте» сильно отличается и потенциально менее надежен, чем прямой сбор проб с помощью метода прямого личного сбора. Несмотря на это, FDA утверждает, что у него есть «самый высокий мировой стандарт отбора проб и тестирования".
Кроме того, FDA предлагает дальнейшее развитие своей политики дистанционного тестирования по почте с помощью недавно предложенный руководящий документ.
Хотя он существует только в виде «проекта» документа FDA, официальные сайты FDA показывают, что рассылка образцов, судя по всему, уже осуществлена как минимум с января 2021 года.. FDA, похоже, утверждает результаты этих присланных по почте тестов как независимую проверку.
Кроме того, нижняя часть первой страницы проекта FDA Документ предлагает расширить «дистанционное тестирование». В настоящее время он перечисляет каждую Подразделение FDA по регулированию продукции FDA, подразумевая, что это политическое предложение всего агентства.
Полный список включает в себя:
- Управление по вопросам регулирования
- Управление продовольственной политики и реагирования
- Офис комбинированной продукции
- Центр оценки и исследований биологических препаратов
- Центр оценки и исследования лекарственных средств
- Центр устройств и радиологического здоровья
- Центр безопасности пищевых продуктов и прикладного питания
- Центр табачных изделий
- Центр ветеринарной медицины
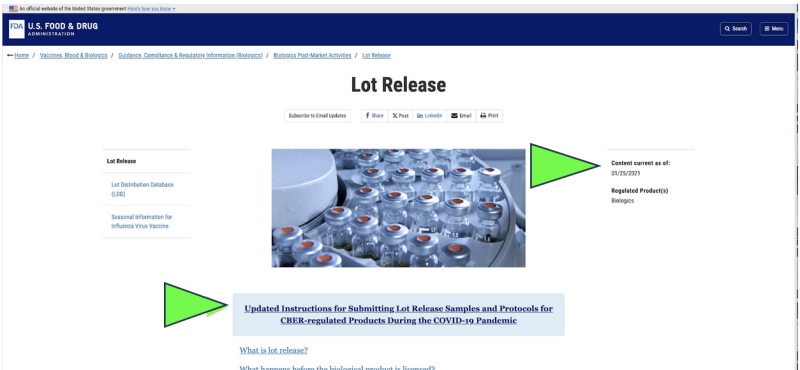
Подходят ли образцы для контроля качества, отправленные по почте FDA? Что, если проверки ресторанов Департамента здравоохранения штатов отражают политику FDA?
Эта методология отбора проб «по почте» столь же абсурдна, например, когда департамент здравоохранения штата контролирует рестораны, прося их периодически «отправлять по почте» различные блюда из своего меню в центр тестирования, чтобы департаменты здравоохранения могли проверить наличие потенциальных продуктов питания. - врожденное заражение и/или требование к ресторанам пообещать самим протестировать пункты меню. Что, если этот ресторан находился в Китае? Что, если этот ресторан находился в Индии? Или любая другая страна, известная наличием ужасная история мошенничества и контроля качества проблемы?
Такая методология была бы неприемлема как для ресторанов, так и для фармацевтических компаний по очевидным причинам: производители могли бы присылать те образцы, которые они предпочитают, – не обязательно репрезентативные образцы партий. Очевидно, это не то же самое, что инспекторы FDA, собирающие образцы во время необъявленных проверок всего объекта.
По аналогии с рестораном, конечно, все рестораны будут предоставить образцы класса «А» который не обязательно будет репрезентативным для того, что получают потребители.

Контроль качества: что такое фармацевтическое «релиз-тестирование» и почему это важно?
Сегодня FDA контролирует качество и содержание $2.7 триллион стоимость продукции в год, но, похоже, скрывает оценки и результаты проверки критических ингредиентов. FDA должно защищать американцев, проводя комплексный аналитическое тестирование в качестве контрольной суммы для обеспечения точности ингредиентов. Результаты этого должны быть прозрачными для налогоплательщиков, которые финансируют $6.6 млрд FDA бюджет. Такая научная проверка называется фармацевтической».тестирование релиза». Тестирование выпуска — это технический термин, обозначающий процесс, включающий различные инструментальные анализы, используемые для всесторонне проверять продукты на чистоту, концентрацию, консистенцию, идентичность и наличие примесей любого рода.
Все FDA родилось из одного сотрудника «Химического департамента» с 1862 года и необходимости прозрачности и проверки ингредиентов. Сегодня этот сотрудник превратился в весь отдел FDA, состоящий из 1,300 ученых и вспомогательного персонала предположительно предназначен для проверки ингредиентов посредством тестирования выпуска фармацевтических препаратов. FDA Управление фармацевтического качества (OPQ) должен гарантировать, что фармацевтические препараты точно соответствуют содержанию перечисленных ингредиентов, без изменений качества/примесей (качественных) или содержания (качественных). Правила, требующие этого, очень конкретны и подробно описаны в 21 CFR § 201.10.
Как FDA проверяет инъекции мРНК для контроля качества:
Результаты контроля качества тестов с инъекциями мРНК были особенно важны, поскольку они большие, сложные и были сделаны быстро. Хотя налогоплательщики зависят от FDA в проверке качества инъекций мРНК и обмене результатами, FDA кажется обязан защищать ингредиенты производителей за счет даже самой элементарной прозрачности в отношении продуктов с мРНК Covid. Хотя FDA, похоже, собирает образцы, их метод «рассылки по почте» в корне ошибочен. Кроме того, FDA не публикует результаты этих тестов нигде, где я мог бы их найти.
Другими словами: во время пандемии, когда совершенно новые, широко применяемые инъекции мРНК навязывали американцам с «фантастической скоростью» и когда Америка больше всего полагалась на обязанности FDA по обеспечению качества и регулированию, FDA принимало самостоятельные «отправленные по почте» в» контроль качества тестирования и/или результатов. Разве FDA не учло это? Производители мРНК признали, что им «изо всех сил [d]» реагировать на производство, и они «изо всех сил стараются» не отставать с производственными процессами? Производители ингредиентов мРНК далее заявили, что усилия по удовлетворению потребностей были «беспрецедентными».
Подобные заявления не приносят потребителям уверенности в качестве и иллюстрируют колоссальное расширение масштабов этих сложных продуктов, которое должно гарантировать особенно бдительный и личный контроль FDA объектов и производимой продукции, независимо от того, пандемия она или нет. Например, один производитель ингредиентов мРНК заявил, что они внезапно увеличили производство на 50 раз.
В разгар этой новой технологии, продвигаемой с «варп-скоростью», никто из 1,300 ученых OPQ в FDA не требовал проведения проверок в реальном времени или, по крайней мере, не предлагал сделать что-либо, кроме запроса потенциально сомнительных «отправленных по почте» образцов. для тестирования?
Очевидный вопрос: почему FDA не собрало образцы напрямую? Даже при наличии пандемии FDA могло бы проверять учреждения в защитных костюмах или – или в очень реже всего – предпочли собирать образцы в аптеках, больницах или на складах дистрибьюторов.
Скрытая методология тестирования ингредиентов для инъекций мРНК:
Помимо отсутствия результатов тестирования и сомнительных результатов «присланных по почте» образцов, FDA дополнительно сокрытие своей проверенной методологии, не позволяющее другим проводить собственный, независимый анализ качества/чистоты инъекций мРНК.
Независимый анализ лекарств на чистоту и потенциальное загрязнение по сравнению со списком ингредиентов — это то, что я пытался сделать сам, когда разрабатывал концепцию первого в мире аналитическая аптека. Однако, поскольку инъекции мРНК представляют собой новую технологию с не совсем прозрачным списком ингредиентов, методология тестирования, которую необходимо будет использовать, не является простой, как это было бы для других низкомолекулярных лекарств. Любой, кто пытается выяснить условия хранения, стабильность, специфичность, химический состав, чувствительность или даже базовую методологию проверки и/или результатов, блокируется отчетом FDA, содержащим смехотворно агрессивные поправки, что делает даже самое фундаментальное научное понимание того, как потенциально оценить результаты или провести тестирование невозможно.
Яркий наглядный пример: одна отредактированная страница в более длинном своде правил FDA (показанном ниже) является частью документ 127-страница (из них только 63 страницы были опубликованы, и из этих 63 страниц около 50% отредактировано) о том, как оценить чистоту, концентрацию и другие аналитические показатели инъекций мРНК.
Те Редакция FDA (b)(4) указаны подробные редакции, используемые для «защищать коммерческую тайну и конфиденциальную коммерческую или финансовую информацию». Но действительно ли уместно называть это «коммерческим», если исследование/разработка/продукт финансировались сотни миллионов долларов налогоплательщиков?

Без списка ингредиентов или методологии тестирования никто, кроме FDA или производителей, не сможет точно знать, как проверять продукт. и фальсификации (измененные или токсичные ингредиенты) или неправильная маркировка (поскольку полный список ингредиентов, включая нуклеотидную последовательность и конфигурации липидных наночастиц особенно расплывчаты на этикетке продукта).
Отсутствие методологии особенно проблематично, поскольку новые предварительные данные, полученные с использованием независимой методологии, свидетельствуют о Контаминация ДНК в инъекциях мРНК Covid.
Таким образом, если посторонний человек заявит, что провел тестирование и обнаружил примесь в уколах мРНК, и попросит FDA или производителей дать ответ, он получит некоторый ответ, в котором будет указано что-то вроде:
- Вы не использовали проверенную/подходящую методологию тестирования, чтобы прийти к своим выводам, и поэтому ваш анализ недействителен.
При этом независимая лаборатория попытается запросить методологию тестирования из документации, одобренной FDA (т. е. полного документа, содержащего фигура 5) спросив: «Хорошо, я хотел бы протестировать по вашей утвержденной методике; ты нам расскажешь, что это такое?»
- FDA или производитель ответят что-то вроде: «То, что мы готовы раскрыть в отношении используемой методологии и не является конфиденциальным, можно найти в Интернете или по запросу FDA FOIA.«…где их встретят следующий сильно отредактированный документ, где все, что хоть сколько-нибудь значимо, покрыто поправками (b)(4).
Читая между строк: очевидно, что и производители, и американское FDA не хотят, чтобы кто-либо, кроме них самих, знал полный состав ингредиентов или даже проверял инъекции мРНК на чистоту и консистенцию.
По словам представителей FDA: Фармацевтическое производство Высоко Склонен к ошибке:
Много что-то может пойти – и действительно – пойти не так в процессе фармацевтического производства. Помимо потенциальных несоответствий с инъекциями мРНК/ЛНП, возникают качественные и количественные проблемы. каждую Фармацевтический продукт, регулируемый FDA. Даже Палата представителей и Сенат официально признали сообщения о неспособности FDA обеспечить безопасность фармацевтической цепочки поставок в Америке. На betXNUMX есть большой выбор Американская фармацевтика продукт для конечного потребителяпроизводится за границей в таких странах, как Индия и Китайи другие страны с низкой стоимостью рабочей силы не ценится за высокий уровень контроля качества. Федеральный реестр пронизан сообщениями о нарушения на индийских и китайских заводах-производителях.
Проводит ли FDA также сертификацию этих растений – в том числе тех, которые имеют давнюю историю нарушений – через систему «почтовой рассылки» в FDA? Возмутительно, но ответ на этот вопрос может поставить в неловкое положение любого, кто обеспокоен качеством фармацевтической продукции.
В то время как Шесть сигм Уровень точности уже давно является целью обеспечения качества и безопасности в производстве автомобилей, компьютеров, мобильных телефонов и других высокотехнологичных производств; похоже, что в фармацевтическом производстве его по большей части упускают из виду.
Представители FDA опубликовали данные, оценивающие погрешность в фармацевтическом производстве в 2-3σ (сигма). Качество 2σ соответствует 308,537 1,000,000 дефектов на XNUMX XNUMX XNUMX возможностей. (Вероятно, когда дело касается фармацевтического производства, существует гораздо больше, чем 1,000,000 XNUMX XNUMX возможностей для ошибок.) FDA знает об этом на самых высоких уровнях руководства; на самом деле, нынешний Глава Управления фармацевтического качества FDA Майкл Копча даже написал и опубликовал приведенный выше расчет «Шесть сигм», сокрушаясь по поводу неточной природы фармацевтического производства. еще в 2017.
Диапазон ошибок для продуктов мРНК и/или их ЛНП может быть даже Меньше точнее, чем 2-3σ (чем ниже σ, тем более ошибочен продукт), поскольку они включают нуклеотидный материал и новые ЛНЧ, что делает их существенно более сложными, чем низкомолекулярные фармацевтические препараты, несмотря на то, что они разрабатываются, производятся и выпускаются с Скорость деформации."
Даже FDA и его чиновники признают присущую производственную неточность. почему в широком мире спорта Разве FDA не выполняет свою миссию по обеспечению безопасности, публично делясь результатами тестирования технологии мРНК с американской общественностью, которая их финансирует?
Опять до 1862 года? Являются ли инъекции мРНК единственными лекарствами, которых нет у американцев? Завершенный Информация об ингредиентах?
Отсутствие ясности относительно количества последовательностей доз мРНК и другой важной информации находится в прямом противоречии с другим одобренным FDA препаратом на основе РНК – патисиран (Онпаттро®). Onpattro прозрачно предоставляет последовательность, молекулярную массу и силу своей продукции в миллиграммах в рамках официального FDA. маркировка упаковки как показано в отрывке ниже:


Отсутствие специфичности дозы мРНК Covid: 0.3 мл (или 0.5 мл) которого?
На данный момент у нас до сих пор нет базовой информации об ингредиентах ни одной инъекции мРНК Covid. Фармацевты умеют давать только конкретные объем жидкости и, по-видимому, сделал это без вопросов. Обычно на официальной маркировке упаковки FDA должны быть указаны фактические ингредиенты в этом объеме, но не на этикетках мРНК Covid: на них просто указывается 0.3 мл (или 0.5 мл) как «Лекарственная форма и дозировка».
Кроме того, любой старшеклассник скажет вам, что 0.3/0.5 мл — это объемне прочность. Мы не знаем никаких количественных особенностей того, что содержится в этих 0.3/0.5 мл, например: сколько частиц ЛНП? Каков размер/морфология этих ЛНП? Сколько последовательностей мРНК в этом объеме?




Это то, что FDA считает достаточно прозрачной или «правдивой маркировкой»?
Приведенная выше выдержка из вкладыша в упаковку представляет собой всю информацию, которой производители делятся с потребителями относительно дозы (которая крайне недостаточна по сравнению со всеми другими этикетками FDA) или с теми, кому интересно узнать что-либо, кроме количества жидкости. для инъекции и концентрацию 30 или 100 мкг неуказанной последовательности мРНК.
Замечательная неточность этой маркировки, разрешенная FDA, кажется, конкретно противоречит ее почти 120-летней маркировке: «требование, чтобы продукты питания и лекарства имели правдивую информацию на маркировке и соответствовали определенным стандартам чистоты и прочности.".
Это то, что FDA считает «правдивым» списком ингредиентов? (Видеть 21CFR §352и 21 Свода федеральных правил, §201.10 относительно «указаний об ингредиентах» и «лекарственных препаратов и устройств с неправильной маркировкой».)
Вопрос в том, является ли перечисление неизвестных или неспецифических ингредиентов, которые никто, кроме производителя, не может расшифровать на самом деле соответствовать духу или юридическим требованиям «маркировки?» Американское FDA считает эту этикетку «правдивой»? На чьей стороне вообще FDA? производители или потребители?
Помимо того, что это не указано напрямую, точное количество нитей ЛНП или мРНК в инъекции 30 или 100 мкг невозможно даже экстраполировать. стехиометрически или на основании Номер Авогадро, поскольку последовательность мРНК, молекулярная масса и/или компонент/конфигурация LNP не указаны нигде в официальной маркировке FDA.
Как можно узнать, пропорционально ли количество нитей мРНК, кодирующих шиповидный белок Covid, нагрузке инокулята Covid, который можно получить от внебольничной инфекции? Отвечать: они не могут.
Являются ли инъекции мРНК Covid Надлежащая маркировка/неправильная маркировка?
21 CFR 211.125 указывает «Строгий контроль осуществляется за маркировкой, выдаваемой для использования в операциях по маркировке лекарственных препаратов,Но, похоже, FDA было настолько небрежно относиться к одобренной маркировке инъекций мРНК Covid, несмотря на то, что любой другой препарат, включая Onpattro на основе мРНК, содержит эту информацию.. Исторически сложилось так, что регуляторные решения FDA (например, какую информацию включать в маркировку продукта) основываются на приоритете, а инъекции мРНК Covid были очевидным отклонением от исторического и юридического приоритета FDA. Это примечательное отсутствие данных и неясность как бы восходят к временам Кордиал Морли для печени и почек в конце 1800-х годов. Разница в том, что тогда FDA не существовало, а сегодня есть FDA, в котором работают около 20,000 XNUMX человек, по крайней мере некоторые из которых якобы верят, что этот ярлык прозрачен и «правдив».
Утверждение неизвестного/неразборчивого/неясного ингредиента, который никто никогда не сможет точно определить, скорее всего, не является тем, чего хотели законодатели Закона о чистых продуктах питания и лекарствах 1906 года, когда они уточняли правила FDA о «правдивой маркировке». Отдельно: то, что дозы у разных производителей увеличены в два раза на объем(30 мкг/0.3 мл vs 100 мкг/0.5 мл) означает, что эти последовательности мРНК сильно различаются по длине нуклеотидов и, в свою очередь, будут иметь все больше и больше LNP плюс вложения. Означает ли это, что последовательности мРНК, используемые для транскрипции белка-шипа, примерно в два раза больше (10 мкг/0.1 мл против 20 мкг/0.1 мл) по сравнению с последовательностями разных производителей, или что-то еще способствует разнице в длине нуклеотидов?
Для непрофессионала, дочитавшего до этого момента (кстати, спасибо): отсутствие подробной информации на маркировке может быть похоже на широкую рекламу дома на продажу, заявляющую, что он построен из дерева и кирпича, на цементной плите – но не показывающую любые фотографии дома (например, последовательность), не разделяющие его площадь (например, молекулярный вес). В любом случае отсутствие информации является недостаточным и является отклонением от традиционных стандартов.
Все остальные лекарства, одобренные FDA, включая другие препараты мРНК, содержат полную информацию о составе своих продуктов, в том числе структурное представление и молекулярная масса своего продукта, чтобы люди точно знали, что они получают.
Это правда: поищите любой наркотик, о котором вы можете подумать, в База данных Drugs.com и обратите внимание, как на всех этикетках указана структура и/или молекулярная масса. Доказательство того, что инъекции мРНК Covid — это бросающийся в глаза исключение из исторической практики одобрения FDA и правила «правдивой этикетки».
Подробности датского исследования 2023 года о значительной клинической вариабельности между партиями инъекций мРНК Covid-19:
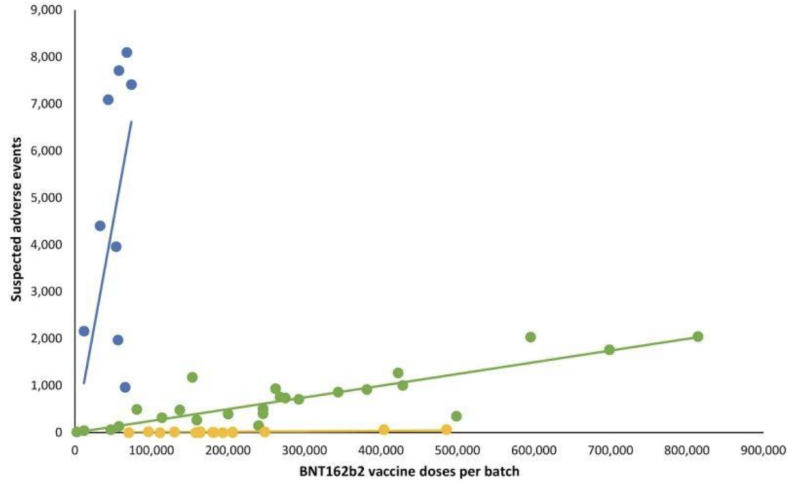
Отсутствие какой-либо прозрачности даже в отношении потенциально недействительных подтверждений результатов тестирования, отправленных по почте, по-видимому, дало производителям возможность пройти еще одну критически важную часть того, за чем наблюдает FDA: потенциальные клинические проявления при вариациях партий мРНК. Ретроспектива Датское исследование безопасности В опубликованной ранее в 2023 году модели отчетов о нежелательных явлениях, связанных с инъекциями мРНК BNT162b2 компании Pfizer-BioNTech, подробно описывается весьма противоречивая картина, коррелирующая с датской системой сообщения о нежелательных явлениях DKMA.
На приведенном ниже линейном графике точки разного цвета обозначают разные партии инъекций мРНК компании Pfizer-BioNTech. Он разделил партии на три разные категории; от высокого-низкого до (почти) отсутствующего количества зарегистрированных групп нежелательных явлений (синий, зеленый и желтый графики соответственно).
Другими словами: предположительно «эквивалентные» продукты одного и того же производителя, похоже, имеют совершенно разную частоту побочных эффектов в зависимости от партии, причем каждая из этих партий представляет собой сотни тысяч инъекций мРНК.
Когда были добавлены соответствующие линии линейной регрессии, возникла определенная закономерность:
Важные вопросы о заслуживающих внимания различиях в нежелательных явлениях между партиями мРНК Covid-19 включают в себя:
- Могут ли отклонения в нежелательных явлениях быть обусловлены качественными или количественными различиями в последовательностях мРНК или количестве нитей мРНК между партиями?
- Могут ли различия в нежелательных явлениях быть следствием качественных или количественных различий в размере/морфологии или количестве ЛНЧ между партиями? Какие анализы были проведены обеспечить безопасность различных ЛНП используется для инъекций мРНК?
- Были ли те партии, которые соответствовали точкам данных желтого, зеленого и синего, каким-то образом качественно или количественно отличались?
- Было ли нарушено хранение/обработка после производства на управляющем предприятии (или где-то еще в цепочке поставок), что привело к изменчивости продукции?
- Какова частота сигм/ошибок для этого и других продуктов, выпускаемых конкретным производственным предприятием/начальником смены, отвечающим за производство?
- Были ли ингредиенты продуктов мРНК Covid получены из Индии или Китая, а не из других стран, в зависимости от партии?
- Какой процент партий продуктов мРНК Covid был проверен инспектором FDA путем личного сбора, а какой процент партий был «отправлен по почте» с момента создания и до настоящего времени? Была ли каждая партия протестирована с использованием только одного из этих двух методов сбора?
- Провело ли FDA проверку выпуска партий датской системы отчетности о нежелательных явлениях DKMA? Если да, то почему FDA не публикует результаты этих конкретных испытаний? Если нет, то почему не было проведено тестирование?
- Существует ли фундаментальная проблема с постоянным получением последовательностей LNP и/или мРНК, надежным и без загрязнения?
Результаты датского исследования и вышеупомянутые вопросы о побочных эффектах могли бы *начать* рассматриваться, но не без того, чтобы FDA независимо поделилось результатами своих исследований выпуска. В нынешнем виде из-за повсеместных поправок FDA (b)(4) никто не знает проверенной методологии тестирования инъекций мРНК Covid. or какие именно партии в датском исследовании были или не были протестированы or результаты этих серийных испытаний.
…С другой стороны, даже если FDA решило опубликовать результаты испытаний этих партий, как потребители узнают, являются ли эти результаты репрезентативными для указанных партий, поскольку производители самостоятельно выбирают, какие образцы «отправлять по почте»?
Отсутствие прозрачности ингредиентов и обеспечения качества с помощью соответствующей методологии отбора проб является фундаментальным и основным требованием FDA. Фактически, это была основная причина создания FDA! Разве американцы не заслуживают большей прозрачности, контроля и «правдивой маркировки» законов, когда дело касается наших фармацевтических препаратов – особенно с учетом того, что эти законы были приняты более 100 лет назад?
Опубликовано под Creative Commons Attribution 4.0 Международная лицензия
Для перепечатки установите каноническую ссылку на оригинал. Институт Браунстоуна Статья и Автор.